https://latamnews.lat/20210604/empieza-reunion-de-regulador-brasileno-que-decidira-importacion-de-vacunas-sputnik-v-1112922257.html
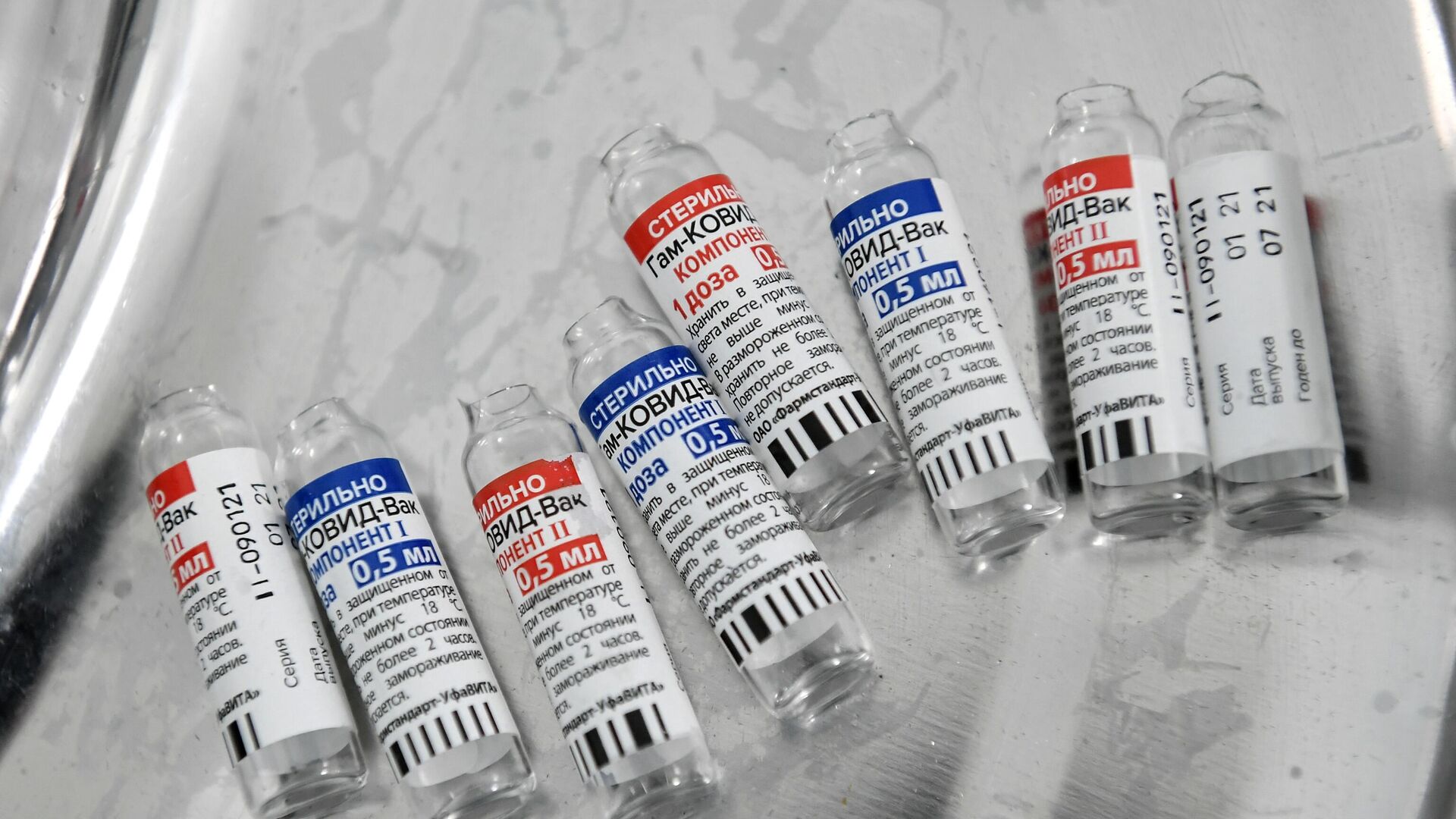
Empieza reunión de regulador brasileño que decidirá importación de vacunas Sputnik V
Empieza reunión de regulador brasileño que decidirá importación de vacunas Sputnik V
Sputnik Mundo
RÍO DE JANEIRO (Sputnik) — La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) empezó la reunión que decidirá sobre dos nuevas peticiones para... 04.06.2021, Sputnik Mundo
2021-06-04T17:42+0000
2021-06-04T17:42+0000
2021-08-09T14:41+0000
américa latina
brasil
sputnik v (vacuna)
vacunación contra el covid-19
rusia
https://cdn.img.latamnews.lat/img/07e5/04/08/1110937532_0:43:3073:1771_1920x0_80_0_0_c8778370823db6859a568291d214c687.jpg
La reunión arrancó poco después de las 14 hora local (17:00 GMT) con las palabras del director-presidente de la Anvisa, Antonio Barra Torres, lamentando la muerte de miles de personas en Brasil por COVID-19 y haciendo un llamamiento a la esperanza con la vista puesta en los países que ya están avanzando en la campaña de vacunación.La decisión de importar o no las citadas vacunas la tomarán los cinco directores de la Anvisa: el propio Torres, Meiruze Sousa, Cristiane Jourdan, Romison Rodrigues y Alex Machado.Antes, el personal técnico hará una presentación sobre las nuevas informaciones presentadas por el Instituto Bharat Biotech y el Instituto Gamaleya, respectivos impulsores de las vacunas Covaxin y Sputnik V.Otras peticiones para importar las citadas vacunas ya fueron rechazas en el pasado: el 31 de marzo la agencia negó la importación de las vacunas indias, y el 26 de abril vetó la llegada de la Sputnik V a Brasil.En esos momentos, la agencia reguladora brasileña alegó que faltaban documentos para sacar conclusiones definitivas sobre la eficacia y seguridad de las vacunas.La Anvisa podría aprobar este 4 de junio el uso de la vacuna Sputnik V contra el COVID-19, después de que el área de medicamentos diera su visto bueno con algunas condiciones.Durante la reunión, el gerente general de Medicamentos y Productos Biológicos de la Anvisa, Gustavo Mendes, afirmó que aún hay "dudas técnicas" sobre cómo la vacuna presenta eficacia y seguridad, pero "teniendo en cuenta el escenario de la pandemia" se propone "la adopción de condicionantes en la eventual autorización de la vacuna". Las condiciones que pone este departamento son las siguientes: La Anvisa también pone como condición para autorizar la vacuna en Brasil que no pueda usarse en embarazadas, lactantes, menores de 18 años, personas con enfermedades graves o no controladas, personas con VIH, fiebre, hepatitis B o C, entre otros grupos de riesgo.Mendes empezó su presentación afirmando que el pasado 21 de mayo el Ministerio de Salud de Rusia entregó un documento de 53 páginas con informaciones adicionales sobre la vacuna, y que esas informaciones crean un "nuevo escenario".Actualmente, las únicas vacunas contra el COVID-19 autorizadas en Brasil son la Coronavac (del laboratorio chino Sinovac), la de la Universidad de Oxford y AstraZeneca, la de Pfizer y la de Janssen.
https://latamnews.lat/20210603/eeuu-china-o-rusia-que-vacunas-prefiere-america-latina--1112818261.html
brasil
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
2021
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
Noticias
es_ES
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
brasil, sputnik v (vacuna), vacunación contra el covid-19, rusia
brasil, sputnik v (vacuna), vacunación contra el covid-19, rusia
Empieza reunión de regulador brasileño que decidirá importación de vacunas Sputnik V
17:42 GMT 04.06.2021 (actualizado: 14:41 GMT 09.08.2021) RÍO DE JANEIRO (Sputnik) — La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) empezó la reunión que decidirá sobre dos nuevas peticiones para importar vacunas contra el COVID-19: la india Covaxin y la rusa Sputnik V.
La reunión arrancó poco después de las 14 hora local (17:00 GMT) con las palabras del director-presidente de la Anvisa, Antonio Barra Torres, lamentando la muerte de miles de personas en Brasil por COVID-19 y haciendo un llamamiento a la esperanza con la vista puesta en los países que ya están avanzando en la campaña de vacunación.
La decisión de importar o no las citadas vacunas la tomarán los cinco directores de la Anvisa: el propio Torres, Meiruze Sousa, Cristiane Jourdan, Romison Rodrigues y Alex Machado.
Antes, el personal técnico hará una presentación sobre las nuevas informaciones presentadas por el Instituto Bharat Biotech y el Instituto Gamaleya, respectivos impulsores de las vacunas Covaxin y Sputnik V.

3 de junio 2021, 19:22 GMT
Otras peticiones para importar las citadas vacunas ya fueron rechazas en el pasado: el 31 de marzo la agencia negó la importación de las vacunas indias, y el 26 de abril
vetó la llegada de la Sputnik V a Brasil.
En esos momentos, la agencia reguladora brasileña alegó que faltaban documentos para sacar conclusiones definitivas sobre la eficacia y seguridad de las vacunas.
La Anvisa podría aprobar este 4 de junio el uso de la vacuna Sputnik V contra el COVID-19, después de que el área de medicamentos diera su visto bueno con algunas condiciones.
Durante la reunión, el gerente general de Medicamentos y Productos Biológicos de la Anvisa, Gustavo Mendes, afirmó que aún hay "dudas técnicas" sobre cómo la vacuna presenta eficacia y seguridad, pero "teniendo en cuenta el escenario de la pandemia" se propone "la adopción de condicionantes en la eventual autorización de la vacuna".
Las condiciones que pone este departamento son las siguientes:
que las vacunas se usen en el marco de un estudio de efectividad que debe ser supervisado por la Anvisa,
que los lotes que lleguen a Brasil procedan de las plantas de producción que esta agencia ya supervisó en Rusia,
que sean revisados por el Instituto Nacional de Control de Calidad de Salud para demostrar que no albergan adenovirus replicantes.
La Anvisa también pone como condición para autorizar la vacuna en Brasil que no pueda usarse en embarazadas, lactantes, menores de 18 años, personas con enfermedades graves o no controladas, personas con VIH, fiebre, hepatitis B o C, entre otros grupos de riesgo.
Mendes empezó su presentación afirmando que el pasado 21 de mayo el Ministerio de Salud de Rusia entregó un documento de 53 páginas con informaciones adicionales sobre la vacuna, y que esas informaciones crean un "nuevo escenario".
Actualmente, las únicas vacunas contra el COVID-19 autorizadas en Brasil son la Coronavac (del laboratorio chino Sinovac), la de la Universidad de Oxford y AstraZeneca, la de Pfizer y la de Janssen.