https://latamnews.lat/20201215/la-ema-decidira-sobre-autorizacion-de-la-vacuna-de-pfizer-y-biontech-el-21-de-diciembre-1093835213.html
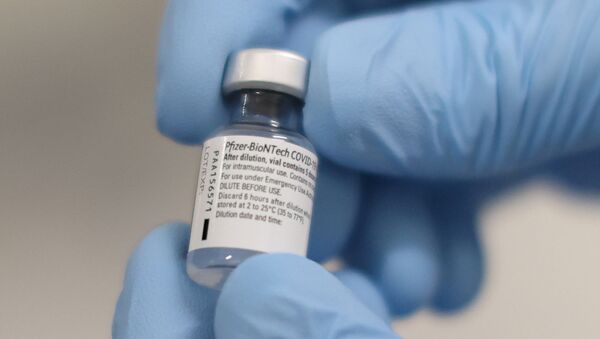
La EMA decidirá sobre autorización de la vacuna de Pfizer y BioNTech el 21 de diciembre
La EMA decidirá sobre autorización de la vacuna de Pfizer y BioNTech el 21 de diciembre
Sputnik Mundo
BRUSELAS (Sputnik) — La Agencia Europea de Medicamentos (EMA) informó que convocará el próximo 21 de diciembre el Comité de Productos Médicos para Uso Humano... 15.12.2020, Sputnik Mundo
2020-12-15T14:09+0000
2020-12-15T14:09+0000
2021-10-07T11:35+0000
💗 salud
sociedad
noticias
vacunación contra el covid-19
pfizer
covid-19
autorización
vacunación
https://cdn.img.latamnews.lat/img/07e4/0c/0c/1093810316_0:94:1841:1134_1920x0_80_0_0_3009e4e10c116a028991fb9a3c222443.jpg
Añadió que la reunión prevista para el 29 de diciembre se celebrará si fuera necesario."El CHMP completará la evaluación lo más rápido posible solo si los datos sobre la calidad, la seguridad y la eficacia de la vacuna son lo suficientemente sólidos y completos para determinar si los beneficios superan los riesgos", afirmó.El 30 de noviembre, Pfizer y BioNTech solicitaron a la EMA una autorización de comercialización condicional para su vacuna anticovid BNT162b2, basada en la tecnología del ARN mensajero.Durante el ensayo clínico de fase 3, el fármaco demostró una efectividad del 95%. Entre los principales desafíos que implica el uso de esta vacuna está el transporte y el almacenamiento a temperaturas ultrabajas, aunque las empresas diseñaron una cadena logística para cumplir dicho requisito.
https://latamnews.lat/20201209/es-segura-la-vacuna-pfizer-a-pesar-de-la-muerte-de-2-personas-inoculadas-1093776759.html
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
2020
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
Noticias
es_ES
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
Sputnik Mundo
contacto@sputniknews.com
+74956456601
MIA „Rosiya Segodnya“
💗 salud, sociedad, noticias, vacunación contra el covid-19, pfizer, covid-19, autorización, vacunación
💗 salud, sociedad, noticias, vacunación contra el covid-19, pfizer, covid-19, autorización, vacunación
La EMA decidirá sobre autorización de la vacuna de Pfizer y BioNTech el 21 de diciembre
14:09 GMT 15.12.2020 (actualizado: 11:35 GMT 07.10.2021) BRUSELAS (Sputnik) — La Agencia Europea de Medicamentos (EMA) informó que convocará el próximo 21 de diciembre el Comité de Productos Médicos para Uso Humano (CHMP) para revisar los datos de la vacuna contra el coronavirus elaborada por la estadounidense Pfizer y la alemana BioNTech.
"Tras la recepción anoche de los datos adicionales solicitados por el CHMP a la compañía y a la espera del resultado de su evaluación, la reunión extraordinaria del CHMP fue programada para el 21 de diciembre", comunicó.
Añadió que la reunión prevista para el 29 de diciembre se celebrará si fuera necesario.

9 de diciembre 2020, 16:20 GMT
"El CHMP completará la evaluación lo más rápido posible solo si los datos sobre la calidad, la seguridad y la eficacia de la vacuna son lo suficientemente sólidos y completos para determinar si los beneficios superan los riesgos", afirmó.
El 30 de noviembre, Pfizer y BioNTech solicitaron a la EMA una autorización de comercialización condicional para su vacuna anticovid BNT162b2, basada en la tecnología del ARN mensajero.
Durante el ensayo clínico de fase 3, el fármaco demostró una efectividad del 95%. Entre los principales desafíos que implica el uso de esta vacuna está el transporte y el
almacenamiento a temperaturas ultrabajas, aunque las empresas diseñaron una cadena logística para cumplir dicho requisito.