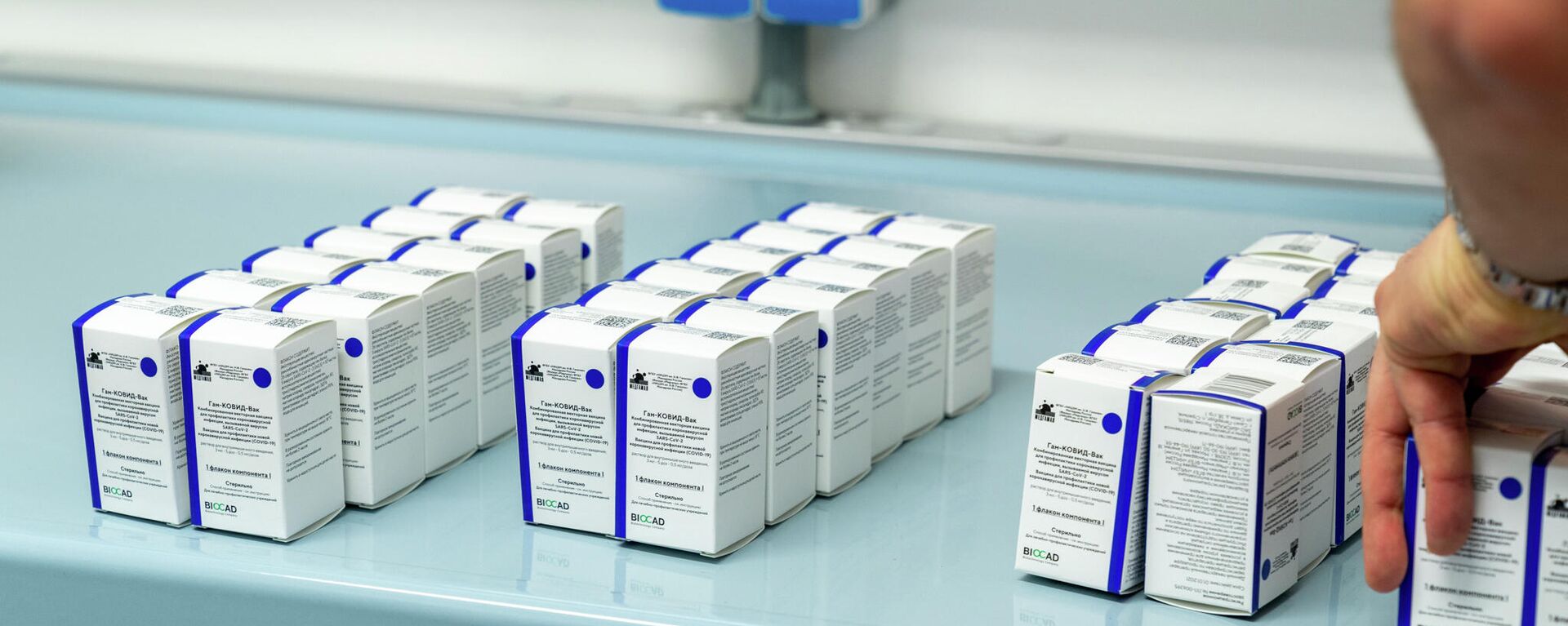
La agencia reguladora de Brasil autoriza a otros 7 estados a importar vacuna Sputnik V
11:36 GMT 16.06.2021 (actualizado: 11:42 GMT 16.06.2021)
© Sputnik / Maxim Bogovid
/ Síguenos en
RÍO DE JANEIRO (Sputnik) — La Agencia Nacional de Vigilancia Sanitaria de Brasil (Anvisa) autorizó la importación de dosis de la vacuna rusa contra el COVID-19 por parte de siete estados que lo habían solicitado.
En un comunicado, este órgano regulador informó que autorizó la "importación excepcional" de la vacuna por parte de los estados de Rio Grande do Norte (noreste), Mato Grosso (centro-oeste), Rondônia (norte), Pará (norte), Amapá (norte), Paraíba (noreste) y Goiás (centro-oeste).
La importación de las vacunas está condicionada a varios requisitos, como que se aplique únicamente a adultos saludables y que se envíen periódicamente a la Anvisa informes de evaluación sobre el riesgo-beneficio de la vacuna.
Otra de las restricciones es que los estados sólo podrán importar dosis por el equivalente al 1% de la población.
De esta forma, los siete estados en conjunto recibirán menos de 600.000 vacunas, repartidas de la siguiente forma:
Pará recibirá 174.000;
Goiás, 142.000;
Paraíba, 81.000;
Rio Grande do Norte, 71.000;
Mato Grosso, 71.000;
Rondônia, 36.000;
Amapá 17.000.
Las limitaciones son las mismas que la Anvisa aplicó a la petición de importación de otros seis estados de la región noreste:
Bahía;
Maranhão;
Sergipe;
Ceará;
Pernambuco;
Piauí.
Esos seis estados recibirán 928.000 dosis en total, que empezarán a llegar a Brasil a principios de julio, según señaló el 15 de junio el gobernador de Ceará, Camilo Santana, tras reunirse con representantes del Fondo de Inversiones Directas de Rusia (RDIF).
Con la autorización de este 16 de junio, 13 de los 27 estados de Brasil ya recibieron la luz verde para poder importar vacunas Sputnik V.


La vacuna rusa Sputnik V
Sputnik V, registrada en Rusia el 11 de agosto de 2020, consta de dos dosis que se aplican con un intervalo de 21 días. La primera se basa en el adenovirus humano tipo 26 y la segunda, en el adenovirus humano recombinante del tipo 5.
A principios de febrero, la revista científica británica The Lancet publicó los resultados provisionales de la tercera fase del ensayo clínico de la vacuna rusa, que confirmaron una seguridad y eficacia del 91,6%.
La vacuna está aprobada en 70 países de Europa, Asia, África y América, entre ellos Argentina, Bolivia, México y Venezuela.