El director de Gamaleya anuncia que los documentos sobre Sputnik V para la EMA están listos
11:34 GMT 05.04.2021 (actualizado: 13:58 GMT 05.04.2021)
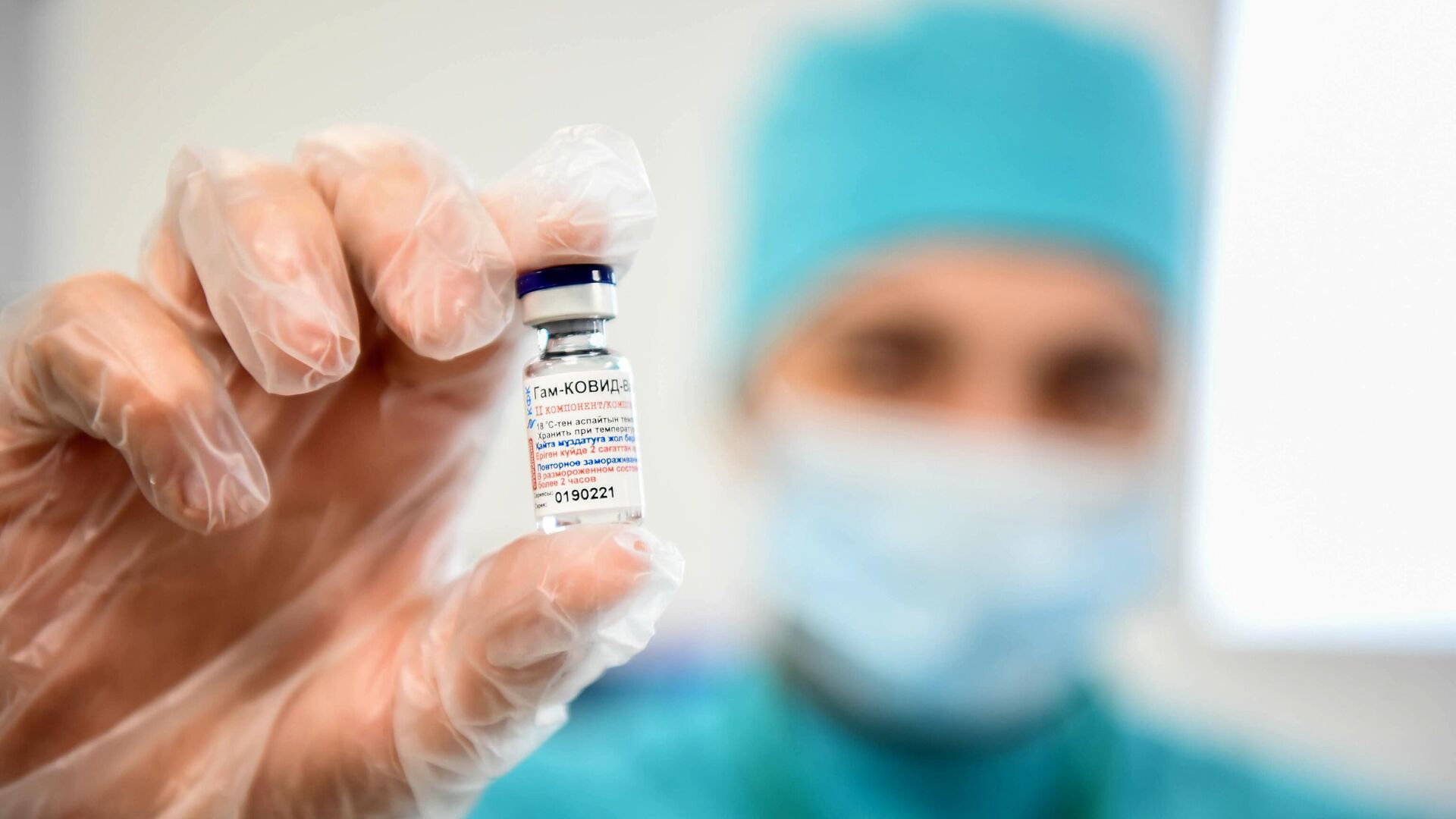
© Sputnik / Vladislav Vodnev
/ Síguenos en
MOSCÚ (Sputnik) — El Centro de Epidemiología y Microbiología Nikolái Gamaleya está preparado para la llegada de los representantes de la Agencia Europea de Medicamentos (EMA), el paquete de documentos sobre la vacuna Sputnik V está listo, declaró en una entrevista con Sputnik el director de la entidad, Alexandr Guíntsburg.
"Siempre estamos listos, siempre estamos abiertos. Se preparó un paquete completo de documentos que pueden interesar a los expertos. Estarán presentes nuestros científicos, que se dedicaron tanto a la preparación de esos documentos como a su redacción directa, y estarán dispuestos a responder a todas las preguntas de los expertos", dijo Guíntsburg.
El ministro de Salud de Rusia, Mijaíl Murashko, anunció previamente que el 10 de abril a Rusia llegará un grupo de expertos de la EMA para monitorear los ensayos clínicos del fármaco ruso contra el coronavirus.
El director de Gamaleya precisó que el personal del centro ya habló en varias ocasiones con expertos de otros países, así como respondió a sus preguntas.
"A todos esos momentos hay que sumarle, además del componente científico, también los aspectos político y económico, relacionados, ya digo, con la promoción de todos esos fármacos en varios mercados, incluido el mercado europeo, un mercado muy rico, según tengo entendido. Por lo tanto, resulta difícil predecir lo que nos espera más adelante, y ni siquiera a nosotros, sino a Sputnik V", enfatizó el experto.
Guíntsburg aseguró que su centro puede garantizar que desde el punto de vista de la ciencia "todo estará bien".


La vacuna rusa Sputnik V
Sputnik V, registrada en Rusia el 11 de agosto de 2020, consta de dos dosis que se aplican con un intervalo de 21 días. La primera se basa en el adenovirus humano tipo 26 y la segunda, en el adenovirus humano recombinante del tipo 5.
A principios de febrero, la revista científica británica The Lancet publicó los resultados provisionales de la tercera fase del ensayo clínico de la vacuna rusa, que confirmaron una seguridad y eficacia del 91,6%.
La vacuna está aprobada en 70 países de Europa, Asia, África y América, entre ellos Argentina, Bolivia, México y Venezuela.
Sigue la versión completa de la entrevista con Alexandr Guíntsburg aquí.


