Comienza la segunda fase de pruebas de la vacuna Sputnik V en la India
14:12 GMT 01.12.2020 (actualizado: 19:57 GMT 11.02.2021)
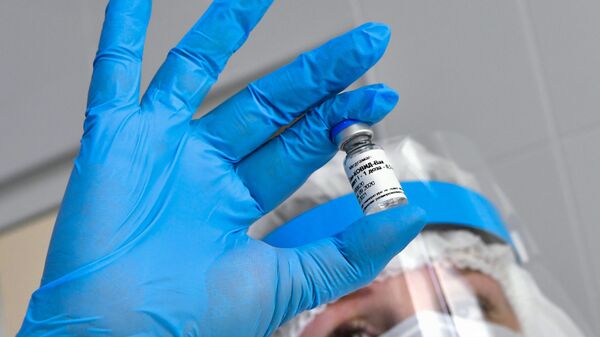
© Sputnik / Georgy Zimarev
/ Síguenos en
MOSCÚ (Sputnik) — La compañía farmacéutica india Dr. Reddy's Laboratories y el Fondo Ruso de Inversión Directa (RDIF, por sus siglas inglesas) comenzaron la segunda fase de los ensayos clínicos adoptivos de la vacuna anticoronavirus rusa Sputnik V en la India, comunicó la empresa del país surasiático.
"Dr. Reddy's Laboratories y el Fondo Ruso de Inversión Directa [RDIF] anunciaron hoy [el 1 de diciembre] que comenzaron la fase 2/3 de los ensayos clínicos de la vacuna Sputnik V en la India", dice el comunicado.
📹 Los laboratorios Dr Reddy's han iniciado las pruebas clínicas de la vacuna rusa contra el coronavirus #SputnikV. Así llega la vacuna a la India 💉🇷🇺
👉 https://t.co/w7kgeiVhrF#VacunaRusa #SputnikV https://t.co/w2Dkv72A2W
👉 https://t.co/w7kgeiVhrF#VacunaRusa #SputnikV https://t.co/w2Dkv72A2W
La nota indica que las pruebas empezaron después de que las autorizara el Laboratorio Central de Drogas, entidad pública encargada de controlar la calidad de los fármacos en la India.
Los ensayos se llevan a cabo por la empresa JSS Medical Research.
El 27 de noviembre pasado el RDIF anunció un acuerdo con la farmacéutica Hetero para fabricar en la India más 100 millones de dosis anuales de la vacuna Sputnik V.

28 de octubre 2020, 11:17 GMT
El pasado 11 de agosto, Rusia registró la primera vacuna contra el COVID-19, llamada Sputnik V y desarrollada por el Centro de Epidemiología y Microbiología Nikolái Gamaleya. El fármaco se produce en cooperación con el Fondo Ruso de Inversión Directa.
Antes del registro, Sputnik V pasó dos fases de pruebas en Rusia, y los ensayos de la fase tres, con la participación de 40.000 voluntarios, se están llevando a cabo en la actualidad.
El 11 de noviembre se anunció que la eficacia de la vacuna Sputnik V es del 92%. La evaluación se basaba en un primer análisis de datos provisionales hecho 21 días después de que a los voluntarios se les administrara la primera dosis y luego de que se confirmaran 20 casos de COVID-19 distribuidos entre el grupo placebo y el grupo inmunizado.
El 24 de noviembre se supo que un segundo análisis intermedio demostró una eficacia de más del 91,4% en el día 28 después de administrada la primera dosis, y del 95% en el día 42.



